Asam Lemah dan Basa Lemah
Asam lemah merupakan senyawa asam yang ketika di dalam air sulit melepaskan ion H+. Selain itu, dalam larutannya mengalami disosiasi sebagian saja. Contohnya seperti:
Sedangkan basa lemah merupakan senyawa basa yang saat berada di dalam air sulit melepaskan ion OH- serta dalam larutannya mengalami disosiasi sebagian. Misalnya seperti:
Larutan Indikator Sintetis
Larutan indikator merupakan zat dengan warna berbeda dalam larutan yang sifatnya asam dan basa. Nah, karena warnanya berbeda, maka larutan indikator sintetis ini bisa kamu gunakan untuk membedakan sifat asam dan basa suatu larutan.
Dari sekian banyak larutan indikator sintetis yang ada, biasanya yang dipakai di laboratorium adalah larutan metil merah, fenolftalein (pp), dan juga metil jingga. Contoh perbedaan asam dan basa menurut larutan indikator sintesis:
PH Meter adalah alat yang mampu mengukur tingkat keasaman atau kebasaan suatu larutan. Cara membedakan asam dan basa melalui alat ini adalah dengan membaca nilai PH-nya.
Jika nilai PH-nya dibawah 7 atau PH < 7 maka larutan tersebut sifatnya asam. Sedangkan jika PH-nya di atas 7 atau PH > 7, maka larutan tersebut sifatnya basa. Sementara itu, jika nilainya 7, berarti larutan tersebut sifatnya netral.
Selain menggunakan peralatan yang ada di laboratorium, kamu juga bisa menggunakan indikator alami yang terdapat pada tumbuhan berwarna. Misalnya seperti daun mahkota bunga, kulit manggis, kunyit, dan lain-lain.
Akan tetapi, untuk menggunakan indikator alami ini kamu harus mengekstrak bahannya lalu ditambahkan dengan air atau larutan, baru bisa dijadikan sebagai indikator. Sebagai contoh, anggaplah kamu ingin menggunakan kulit manggis, maka cara mengidentifikasinya adalah:
Kamu juga bisa memanfaatkan bahan-bahan alami yang warnanya cerah untuk menjadi indikator dalam membedakan sifat asam dan basa. Contohnya seperti bunga sepatu. Jika bunga sepatu dimasukkan ke dalam larutan basa, warnanya akan lebih gelap sedangkan pada larutan asam, warnanya akan jadi lebih muda dan terang.
Temukan contoh indikator alami asam dan basa yang lain dalam buku Kimia Lingkungan yang ditulis oleh Manihar Situmorang. Buku ini membahas tentang pengertian dan istilah-istilah yang sering ditemukan di dalam Kimia Lingkungan, berbagai kasus lingkungan yang berhubungan dengan zat kimia, sifat dan komposisi air, pencemaran air, pengolahan air minum dan pengolahan limbah cair, sifat dan komposisi atmosfer, pencemaran udara, pencemaran darat, dan toksikologi lingkungan.
Asam Kuat dan Basa Kuat
Asam kuat, singkatnya, merupakan senyawa asam yang dapat dengan mudah melepaskan ion H+ di dalam air dan dalam larutannya terjadi disosiasi total. Beberapa contoh asam kuat diantaranya seperti::
Sementara itu, basa kuat merupakan senyawa basa yang dapat dengan mudah melepaskan ion OH- di dalam air dan dalam larutannya terjadi disosiasi total. Misalnya seperti
Klasifikasi Asam dan Basa
Di atas sudah disebutkan bahwa larutan asam dan basa dibagi menjadi dua jenis, yaitu kuat dan lemah. Kira-kira apa maksudnya? Mari kita bahas satu-satu, ya!
Cara Membuat Larutan Asam Dan Basa
Kalau mau, sebenarnya kamu bisa membuat larutan asam dan basa sendiri dengan cara yang cukup mudah. Sebab pada dasarnya larutan asam dan basa bisa kamu dapatkan dengan melarutkan asam maupun basa ke dalam air secara langsung.
Bahkan, kamu bisa mendapatkan larutan ini lewat reaksi antara air dengan senyawa oksida. Reaksi air dengan oksida asam, misalnya, akan menghasilkan larutan asam. Sebaliknya, reaksi air dengan oksida basa akan menghasilkan larutan basa.
Lalu apa yang dimaksud dengan oksida? Ini adalah senyawa yang terbentuk dari oksigen dan unsur tertentu. Untuk menghasilkan oksida asam, kamu bisa memakai oksigen dengan unsur nonlogam seperti P2O5, CI2O7, SO2, atau CO2. Selain itu, ada beberapa reaksi yang dapat menghasilkan larutan asam, diantaranya:
Selanjutnya, larutan basa bisa terbentuk dengan cara mereaksikan air dengan oksida basa. Oksida basa di sini maksudnya adalah jenis oksida yang terbentuk dari oksiden dengan unsur logam, contohnya seperti Fe2O3, Na2O, atau CaO. Nah, contoh reaksi yang menghasilkan larutan basa diantaranya adalah:
Namun perlu kamu tahu, diantara senyawa oksida ada juga yang dikenal dengan oksida indiferen yang tidak bisa menghasilkan asam atau basa. Contohnya seperti NO maupun CO. Lalu ada juga oksida amfoter yang bisa bereaksi dengan ion asam (H+) dan ion basa (OH-). Misalnya ZnO atau AI2O3.
Temukan cara lain untuk membuat larutan asam dan basa dalam buku Kimia SMA/MA Kelas 10 Peminatan Kurikulum 2013 (Edisi Revisi) yang ditulis oleh A Haris Watoni.
Senyawa asam bisa ditemukan dengan mudah dalam kehidupan sehari-hari, namun kita tidak mengetahuinya karena memang kita tidak boleh dan tidak bisa mengujinya secara langsung.
Nah, berdasarkan asalnya, senyawa asam dalam kehidupan sehari-hari dibedakan menjadi beberapa jenis yaitu:
Sama seperti senyawa asam, senyawa basa juga bisa kita temukan dalam kehidupan sehari-hari. Namun senyawa basa lebih mudah dikenali karena sifatnya yang licin dan juga rasanya yang pahit. Nah, beberapa contoh basa diantaranya seperti:
Demikian pembahasan tentang sifat asam dan basa. Semoga semua pembahasan di atas bermanfaat untuk kamu. Jika ingin mencari buku seputar ilmu kimia, maka kamu bisa mendapatkannya di gramedia.com.
Untuk mendukung Grameds dalam menambah wawasan, Gramedia selalu menyediakan buku-buku berkualitas dan original agar Grameds memiliki informasi #LebihDenganMembaca.
Gilang Oktaviana Putra
Sifat-Sifat Logaritma
Logaritma juga memiliki sifat-sifat yang wajib kamu pahami, nih. Kenapa wajib? Oh ya jelas, karena sifat-sifat inilah yang akan menjadi bekal kamu untuk mengerjakan soal-soal logaritma. Tanpa memahami sifat-sifat logaritma, kamu tidak akan bisa mengerjakan soal-soal logaritma, lho!
Lalu, apa saja sih sifat-sifat logaritma dan contohnya? Yuk, kita simak pada gambar di bawah ini!
“Duh, kenapa banyak banget sih sifat-sifat logaritma itu? Males ih ngafalinnya. Ribet!”
Eits… jangan salah, semua sifat di atas pasti bisa kamu kuasai dengan mudah, kok. Caranya, kamu bisa memperbanyak latihan soal tentang logaritma. Tentunya, di aplikasi Ruangguru, dong. Hehehe…
Baca Juga: Bentuk-Bentuk Persamaan Logaritma dan Cara Menyelesaikannya
Oke, supaya kamu jadi paham sifat-sifat logaritma di atas dipakai untuk model soal seperti apa, ayo kita coba kerjakan soal di bawah ini. Kita kerjakan bersama-sama, ya!
Gimana, kamu sudah cukup paham tentang materi logaritma? Sebelum lanjut ke contoh-contoh soal logaritma, misalnya kamu mau mempelajari materi logaritma bareng ahlinya, boleh banget gabung di Ruangguru Privat Matematika.
Di Ruangguru Privat, kamu akan dimentori oleh guru-guru berkualitas yang sudah terstandarisasi. Kamu juga bebas mau pilih belajar secara tatap muka (offline) atau lewat daring (online). Fleksibel banget, kan. Yuk langsung daftar sekarang!
Cara membedakan asam dan basa
Senyawa asam sebenarnya bisa kita temukan dengan mudah pada beberapa buah-buahan, seperti lemon atau jeruk. Selain itu, ada juga di dalam bahan makanan seperti cuka dan pengawet makanan seperti asam benzoat.
Sementara itu, senyawa basa biasanya ditemukan pada benda-benda yang rasanya pahit seperti sabun atau obat. Sekali lagi, meski keduanya identik dengan rasa masam dan pahit, namun sangat tidak dianjurkan untuk membedakan larutan asam dan basa secara langsung. Kalau kamu mau membedakan mana larutan asam dan larutan basa, ada beberapa cara yang bisa kamu lakukan. Berikut penjelasan setiap caranya:
Cara membedakan asam dan basa yang paling sederhana adalah mengujinya memakai kertas lakmus. Kertas lakmus sendiri merupakan kertas indikator yang akan berubah warna saat terkena larutan asam atau basa. Kertas ini terbagi menjadi dua jenis, yaitu lakmus merah dan juga lakmus biru.
Lakmus merah merupakan jenis kertas lakmus yang jika bersentuhan dengan larutan basa akan berubah warnanya menjadi biru. Sedangkan ketika bersentuhan dengan larutan asam, warnanya tetap.
Lakmus biru merupakan jenis kertas lakmus yang jika bersentuhan dengan larutan asam warnanya akan berubah menjadi merah, sedangkan jika bersentuhan dengan larutan basa, warnanya tidak berubah.
Jika kamu ingin menguji sifat dari sebuah larutan dengan menggunakan kertas lakmus merah dan biru, berikut ini ada rangkuman yang membantu mempermudah proses identifikasinya:
Kertas PH Universal, sama seperti kertas lakmus, merupakan indikator berbentuk kertas yang bisa kamu gunakan untuk membedakan asam dan basa. Bedanya kertas ini mempunyai beberapa warna yang menunjukkan skala nilai PH dari larutan yang diuji, mulai dari PH 1 sampai dengan PH 14.
Maka dari itu, dalam pelajaran Kimia, kertas PH Universal bisa digunakan untuk membedakan asam-basa, tetapi juga untuk mengetahui serta mengukur nilai PH dari suatu larutan. Cara kerjanya juga mirip dengan seperti kertas lakmus, yaitu warnanya akan berubah ketika bersentuhan dengan suatu larutan. Warna yang dihasilkan menunjukkan berapa nilai PH dari larutan tersebut.
Jadi, setelah dicelupkan pada sebuah larutan, kertas PH Universal ini akan berubah warnanya. Setelah itu, kamu perlu membandingkan perubahan warna tersebut dengan skala warna PH. Pilihlah warna yang paling sesuai untuk mengetahui berapa nilai PH dari larutan yang kamu uji. Kira-kira seperti ini gambaran skala PH dalam kertas PH Universal:
sciencenewsforstudents.org
Asam bereaksi dengan basa
Pada umumnya, setiap zat yang mempunyai sifat berlawanan cenderung bereaksi antara satu sama lain. Menariknya, reaksi antara asam dan basa menjadi pusat kimiawi sistem kehidupan, lingkungan, serta berbagai proses industri.
Tak hanya itu, reaksi antara kedua larutan ini dapat menghasilkan air dan garam sehingga disebut juga dengan penggaraman. Dari penjelasan ini, bisa disimpulkan bahwa asam dan basa memiliki ciri-ciri sebagai berikut:
Memiliki sifat korosif
Sifat utama lain dari asam dan basa adalah memiliki sifat korosif. Karena itu, larutan asam dapat bereaksi dengan marmer, logam, atau bahan lainnya. Sedangkan basa akan bersifat korosif ketika bersentuhan dengan kulit dan dapat merusak jaringan atau menyebabkan luka bakar. Seperti yang dijelaskan oleh Hardjono Satrohamidjojo dalam bukunya yang berjudul Kimia Dasar Revisi.
Contoh Soal Logaritma dan Pembahasannya
Sekarang, kita coba kerjakan contoh soal logaritma, ya! Perhatikan soal berikut:
Pada soal nomor 1, hal pertama yang harus kita lakukan adalah cek basisnya. Kedua persamaan logaritma di atas, ternyata memiliki nilai basis yang sama, yaitu 2.
Nah, karena basisnya sama, kita bisa menggunakan sifat logaritma yang kedua nih, untuk mengetahui hasilnya. Sehingga, 2log 4 + 2log 8 = 2log (4 × 8) = 2log 32 = 5.
Ingat! tujuan logaritma adalah mencari pangkat. Jadi, 2 pangkat berapa yang hasilnya 32? Jawabannya adalah 5. Mudah, ya? Kita lanjut ke soal nomor 2, yuk!
Pada soal nomor 2 ini, kita tidak bisa langsung mengerjakannya karena kamu pasti akan bingung untuk mencari nilai pangkat dari 8 yang hasilnya 32. Lalu bagaimana?
Kalau kita perhatikan soalnya dengan jeli, 8 itu merupakan hasil pemangkatan dari 23 dan 32 merupakan hasil pemangkatan dari 25. Sehingga, bentuk logaritmanya bisa kita ubah menjadi seperti berikut:
Gimana? sudah mulai greget? Nah, soal nomor 3 ini akan membuat kamu semakin gregetan lagi, nih! Perlu kamu ketahui, model soal nomor 3 akan sering kamu temui pada soal-soal ujian maupun soal-soal seleksi Perguruan Tinggi, lho.
Kelihatannya memang cukup rumit ya, tapi jika kamu telah paham konsepnya, soal ini akan jadi sangat mudah untuk dikerjakan. Jika kamu menemui model soal seperti ini, kamu bisa menyelesaikannya menggunakan sifat logaritma nomor 4.
Sehingga, pengerjaannya akan menjadi seperti berikut:
Note: Untuk memilih basis, kita lihat saja angka yang paling sering muncul pada soal. Angka 2 muncul sebanyak 2 kali, 8 sebanyak 1 kali, dan 7 sebanyak 1 kali. Angka yang paling banyak muncul adalah 2, sehingga kita pilih 2 sebagai basis. Paham, ya?
Selanjutnya, kita uraikan numerusnya. Usahakan kita ubah kebentuk yang sudah ada pada soal. Maksudnya gimana? Begini, di soal diketahui 2log 8 dan 2log 7. Karena numerusnya 8 dan 7, kita uraikan 14 menjadi 7 × 2 dan 16 menjadi 8 × 2 agar kita bisa ketahui hasil akhirnya.
Baca Juga: Belajar Fungsi Komposisi & Contohnya, Lengkap!
Setelah kamu memahami ketiga contoh soal di atas, bagaimana menurutmu? Ternyata logaritma bukanlah materi yang sulit untuk dipahami, ya.
Kamu juga perlu ingat nih, karena tujuan logaritma adalah mencari pangkat, maka modal pertama yang harus kamu miliki adalah hafal perkalian. Setelah itu, kamu juga harus paham dengan sifat-sifat logaritma. Jangan lupa untuk perbanyak latihan soal agar kamu semakin mantap lagi, nih.
Oh ya, di bawah ini ada latihan soal yang bisa kamu kerjakan. Bagi yang tahu, jangan ragu untuk tulis jawabanmu di kolom komentar ya!
Wah, menarik ya pembahasan kali ini. Bagi kamu yang masih kurang paham, kamu bisa lho, belajar lebih lanjut di ruangbelajar. Belajar jadi mudah dan praktis di mana saja dan kapan saja. Yuk, buruan download aplikasinya sekarang!
Sinaga, B. Sinambela, P. N. J. M. Sitanggang, A. K. dkk. (2014). Matematika. Jakarta: Kemendikbud.
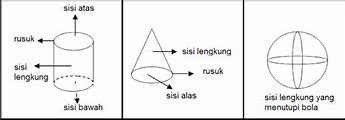
Untuk lebih memahami keunikan tabung, mari kita bandingkan dengan beberapa bangun ruang lainnya:
- Tabung memiliki alas dan tutup yang sejajar dan sama besar, sedangkan kerucut hanya memiliki satu alas dan satu titik puncak.
- Selimut tabung berbentuk persegi panjang jika dibuka, sementara selimut kerucut berbentuk juring lingkaran.
- Volume tabung lebih besar daripada kerucut dengan alas dan tinggi yang sama.
- Tabung memiliki sisi lengkung (selimut), sedangkan semua sisi balok datar.
- Tabung tidak memiliki titik sudut, sementara balok memiliki 8 titik sudut.
- Alas dan tutup tabung berbentuk lingkaran, sedangkan alas dan tutup balok berbentuk persegi panjang.
- Alas dan tutup tabung selalu berbentuk lingkaran, sedangkan prisma bisa memiliki alas berbentuk segitiga, segiempat, atau segi banyak lainnya.
- Tabung tidak memiliki titik sudut, sementara prisma memiliki titik sudut sesuai bentuk alasnya.
- Selimut tabung berbentuk lengkung, sedangkan sisi tegak prisma berbentuk persegi panjang.
- Tabung memiliki alas dan tutup yang datar, sedangkan bola seluruh permukaannya melengkung.
- Tabung memiliki tinggi yang dapat diukur, sementara bola tidak memiliki tinggi.
- Volume tabung dihitung dengan πr²t, sedangkan volume bola dihitung dengan 4/3πr³.
Bicara tentang sifat asam dan basa, rasanya kurang lengkap kalau tidak membahas jeruk dan sabun. Mengapa begitu? Karena keduanya adalah contoh asam dan basa yang bisa kita temukan dengan mudah. Selain itu, di sekolah dulu, banyak guru mengajari bahwa larutan asam, kalau dicicipi, rasanya masam. Sedangkan larutan basa, rasanya pahit. Meski begitu, kita tidak boleh sembarangan mencicipi suatu larutan untuk mengklasifikasikannya.
Lalu, sebenarnya apa itu larutan asam dan basa? Dalam ilmu kimia, yang dimaksud larutan asam merupakan larutan dengan PH < 7 sedangkan larutan basa memiliki PH > 7. Bagaimana kita bisa mengetahui tingkat PH suatu larutan? Ada kok caranya, namun kamu bisa menentukan jenis suatu larutan melalui sifat-sifatnya.
Nah, dalam artikel ini kita akan membahas tentang sifat asam dan basa, ciri-cirinya, dan bagaimana cara membedakan keduanya. Simak baik-baik, ya!